Shaanxi BLOOM Tech Co., Ltd. on yksi Kiinan kokeneimmista eksenatidisuspension valmistajista ja toimittajista. Tervetuloa tukkumyyntiin korkealaatuista eksenatidisuspensiota, joka myydään täällä tehtaaltamme. Hyvä palvelu ja kohtuullinen hinta on saatavilla.
Eksenatidisuspensioon hypoglykeeminen lääke, joka perustuu glukagonin kaltaisten peptidi-1 (GLP-1) -reseptorin agonisteihin ja joka kuuluu peptidiluokkaan. Sen ydinkomponentti, Exenatide, on peptidi, joka koostuu 39 aminohaposta, jotka syntetisoidaan geneettisen rekombinaatioteknologian avulla. Lääkkeen kehittivät alun perin Eli Lilly ja Amlin Pharmaceuticals, ja Yhdysvaltain elintarvike- ja lääkevirasto (FDA) hyväksyi sen markkinoille vuonna 2005, ja siitä tuli ensimmäinen GLP-1-reseptoriagonistilääke.
Tuotteemme lomake







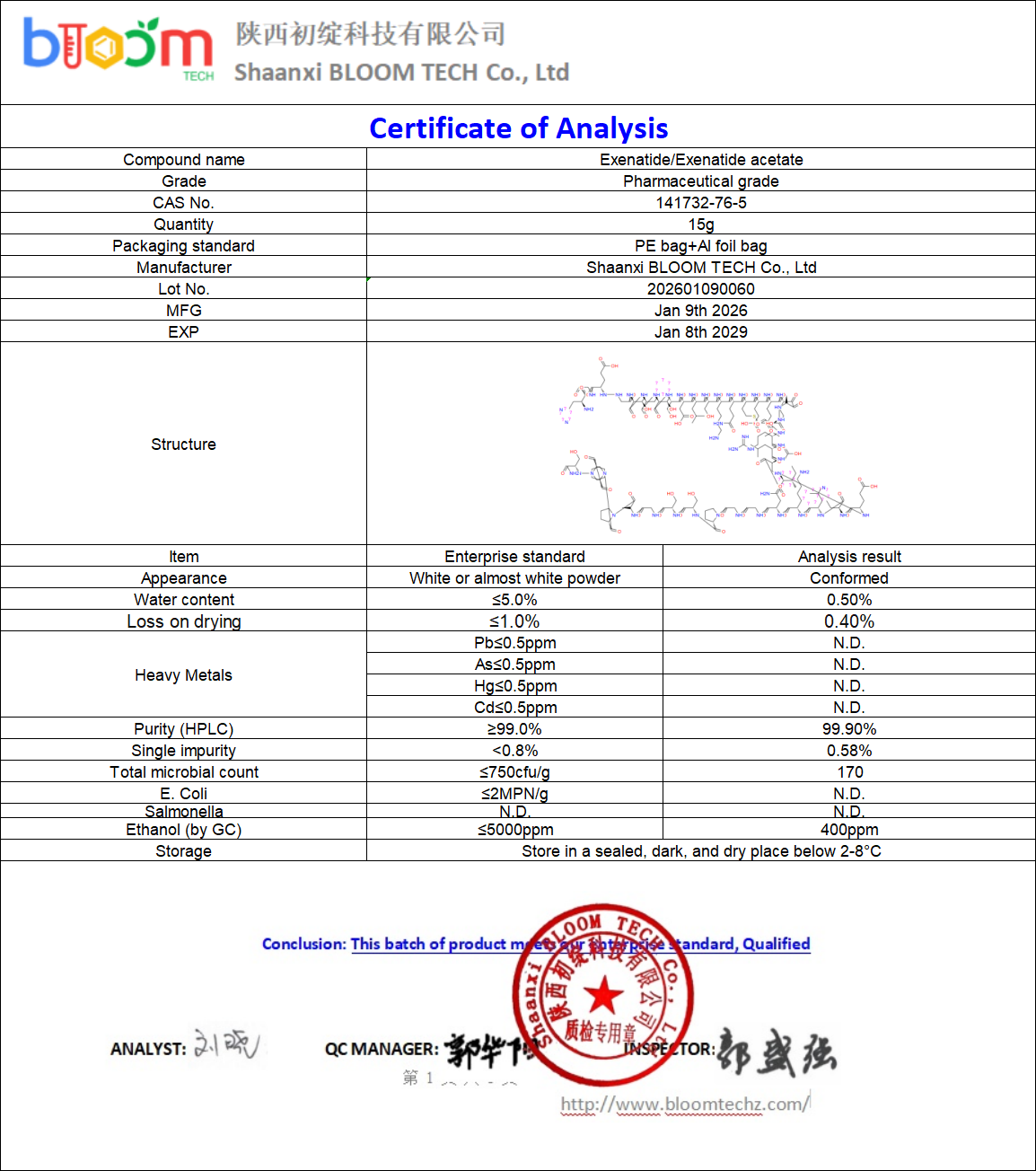
Eksenatidi/eksenatidiasetaatti-COA

Saaristosolujen laadun (määrä ja toiminta) asteittainen heikkeneminen on tyypin 2 diabeteksen keskeinen patologinen piirre. Patologiset tekijät, kuten korkea sokeri, lipiditoksisuus, oksidatiivinen stressi, tulehdus ja endoplasminen verkkokalvon stressi estävät - solujen lisääntymistä ja indusoivat - soluapoptoosia, mikä johtaa toiminnallisten - solupopulaatioiden romahtamiseen.EksenatidisuspensioKlassisena GLP-1-reseptorin agonistina aktivoi kolme ydinsignalointiverkkoa: PI3K Akt, cAMP PKA Epac ja AMPK{5}}SIRT1 alavirtaan GLP-1R:stä, saavuttaen --solulaadun kolminkertaisen tarkkuuden: edistää haiman erilaisten solujen kypsymistä, stimuloi {{tai solujen kypsymistä}}. proliferaatiota ja tehokkaasti inhiboi - soluapoptoosia.
Alkion kehitys ja beetasolujen jakautuminen kudoksiin
Beetasolujen kehitys lähtee endodermista, ja niiden erilaistuminen ja kypsyminen on monivaiheinen, monigeeninen säätelyprosessi, joka tapahtuu pääasiassa alkionkehityksen keski- ja loppuvaiheessa. Synnytyksen jälkeen tapahtuu edelleen tietty määrä lisääntymistä ja kypsymistä.
Haiman primordian muodostuminen
Alkionkehityksen 3.–4. viikon aikana etusuolen endodermin solut erilaistuvat dorsaalisiin ja ventraalisiin haiman silmuihin, jotka ovat haiman kehityksen alkiomuotoja. Tällä hetkellä endokriinisten solujen erilaistumista ei ole vielä tapahtunut.


Endokriinisten esiastesolujen erilaistuminen
Alkion 8.-10. viikon aikana haiman silmussa olevat epiteelisolut erilaistuvat vähitellen monipotenteiksi haiman esiastesoluiksi, jotka erilaistuvat entisestään endokriinisiksi esiastesoluiksi ja alkavat ilmentää haimasoluspesifisiä transkriptiotekijöitä, kuten PDX-1, NKX6.1, PAXn4:n suorat molekyylejä säätelevät tekijät jne. beetasolujen erilaistuminen.
- solujen kypsyminen ja haiman saarekkeiden muodostuminen
12 viikon alkionkehityksen jälkeen endokriiniset esiastesolut erilaistuvat vähitellen epäkypsiksi beetasoluiksi ja alkavat ilmentää insuliinigeenejä; Epäkypsät beetasolut lisääntyvät, vaeltavat ja aggregoituvat nopeasti 20. raskausviikosta syntymään saakka muodostaen rakenteellisesti ehjän haiman saarekkeen yhdessä alfasolujen, deltasolujen ja muiden solujen kanssa. Beetasolut ovat haiman saarekkeen keskeisessä asemassa muodostaen klassisen haiman saarekerakenteen "keskeisistä beetasoluista ja perifeerisistä muista soluista".


Kypsyminen ja lisääntyminen syntymän jälkeen
Vastasyntyneestä nuoruuteen beetasolut jatkavat lisääntymistä ja kypsymistä, ja insuliinin eritystoiminto paranee vähitellen; Aikuisen iän jälkeen beetasolujen lisääntymiskyky laskee merkittävästi, pääasiassa ylläpitämällä vakaata solumäärää. Rajoitettua kompensoivaa lisääntymistä voi esiintyä, kun aineenvaihduntakuormitus lisääntyy (kuten liikalihavuus ja raskaus).
Viitetietolähde:
- Chen Jialun Clinical Endocrinology (2. painos) Shanghai Science and Technology Press, 2011
- Bonner-Weir S. Haiman beetasolun elämä ja kuolema. Diabetestiede ja tekniikka. 2010.
- Finegood DT, Scaglia L, Bonner{0}}Weir S. Beeta-solumassan dynamiikka kasvavassa rotan haimassa. Diabetes. 1995.
- Kahn SE, Hull RL, Utzschneider KM. Mekanismit, jotka yhdistävät lihavuuden insuliiniresistenssiin ja tyypin 2 diabetekseen. Luonto. 2006.
solumassan lasku: tyypin 2 diabeteksen patologinen ydin
- solulaadun fysiologinen säätelyjärjestelmä
Beetasolujen laadun ylläpitäminen aikuisissa organismeissa on dynaaminen tasapainoprosessi, jota säätelee kolme ydinkomponenttia:
--solujen neogeneesi: Haiman tiehyepiteelisolut, akinaarisolut, alfasolut ja muut esiastesolut erilaistuvat toiminnallisiksi --soluiksi, jotka ovat tärkeä --solulisäyksen lähde aikuisiässä.
Beetasolujen lisääntyminen: Kypsät beetasolut replikoivat itsensä mitoosin kautta, joka on tärkein reitti beetasolujen massalaajenemiseen syntymän jälkeen.


Beetasolujen apoptoosi: Yliaktivoituminen patologisissa olosuhteissa johtaa kuolemaan ja beetasolujen määrän vähenemiseen.
Fysiologisissa olosuhteissa nämä kolme ovat tasapainossa toiminnallisten beetasolujen vakaan populaation ylläpitämiseksi; Tyypin 2 diabeteksessa neogeneesi ja proliferaatio estyvät, apoptoosi on hyperaktiivista ja tasapaino on täysin romahtanut.
Glukotoksisuus: Krooninen korkea glukoosi aiheuttaa oksidatiivista stressiä, mitokondrioiden toimintahäiriöitä, endoplasmista verkkostressiä (ERS) ja aktivoi JNK-, p38 MAPK- ja CHOP-apoptoottisia reittejä.
Lipotoksisuus: Vapaiden rasvahappojen (FFA) kerääntyminen indusoi lipidien apoptoosia, mitokondriovaurioita ja insuliinin eritysvirheitä beetasoluissa.
Oksidatiivinen stressiepidemia: Liiallinen ROS:n muodostuminen, joka vahingoittaa DNA:ta, proteiineja ja lipidejä, aktivoi apoptoottisen kaskadin.


Endoplasminen verkkostressi (ERS): Laskeutumattomien proteiinien kerääntyminen aktivoi PERK-eIF2 - ATF4 CHOP -reitin ja indusoi apoptoosia.
Tulehduksellinen vamma: Krooninen matala-asteinen haiman tulehdus, jossa tulehdusta edistävät tekijät, kuten TNF -, IL-1, IFN -, aktivoivat NF-κ B- ja kaspaasi-apoptoottisia reittejä.
IAPP:n epänormaali aggregaatio: haiman amyloidipeptidi on laskostunut väärin muodostaen toksisia oligomeerejä, vaurioittaen beetasolukalvoja ja indusoimalla apoptoosia.
Viitetietolähde:
- Maksan vuorokausirytmiä säätelevän eksenatidin molekyylimekanismin tutkimus. Kiinan farmakologinen tiedote, 2024
- GLP-1-reseptorin agonisti, eksenatidi, antoaika vaikuttaa eri tavalla vuorokausirytmeihin diabeettisissa db/db-hiirissä. Kentuckyn yliopiston lääketieteellinen korkeakoulu, 2024
- GLP-1-reseptoriagonistien säätelyvaikutus ja kliininen merkitys maksan vuorokausirytmiin. Chinese Journal of Endocrinology and Metabolism, 2024
Eksenatidin reseptori- ja signalointireitti säätelee --solumassaa
GLP-1R (G-proteiiniin kytketty reseptori B-perhe) ekspressoituu voimakkaasti haiman beetasolukalvoissa ja sijaitsee organellikalvoissa, kuten endoplasmisessa retikulumissa ja mitokondrioissa, tarjoten rakenteellisen perustan solujen moniulotteiselle säätelylle.eksenatidisuspensio.
Solukalvo GLP-1R: käynnistää solunsisäisen signaalin proliferaation ja apoptoosin säätelemiseksi.
Solukalvo GLP-1R: säätelee suoraan endoplasmista retikulumia ja mitokondrioiden homeostaasia, estää ERS:ää ja oksidatiivista stressiä.

Eksenatidi aktivoi GLP-1R:n kolminkertaisen säätelyydinreitin

Suuren affiniteetin GLP-1R:n kanssa sitoutumisen jälkeen eksenatidi aktivoi kolme suurta ristisynergististä signaaliverkkoa, jotka välittävät tarkasti - solun neogeneesin, proliferaation ja apoptoosin eston:
PI3K Akt-FoxO1-reitti: ydinproliferaatio- ja anti-apoptoottinen reitti, joka edistää sykliini D1:n ilmentymistä, estää FoxO1-, GSK3- ja pro-apoptoottisia proteiineja.
CAMP PKA Epac -reitti: edistää - solujen regeneraatiota, tehostaa insuliinigeenin ilmentymistä, estää ERS:ää ja stabiloi mitokondrioiden kalvopotentiaalia.
AMPK-SIRT1-PGC-1-reitti: säätelee autofagiaa, mitokondrioiden biosynteesiä, antioksidanttistressiä ja parantaa energia-aineenvaihduntaa.
Kolme pääreittiä tehostavat toisiaan: Akt aktivoi AMPK:ta, PKA lisää Akt-aktiivisuutta, SIRT1 deasetyloi FoxO1:n ja PGC-1:n muodostaen kattavan solusuojaverkoston.

Exenatide-solusuojan rakenteellinen perusta

Eksenatidi (eksendiini-4) 39 -peptidillä on beetasoluihin kohdistuva sopeutumiskyky:
Suuriaffiniteettinen sitoutuminen --soluun GLP-1 R, aktivaatiotehokkuudella yli 10 kertaa luonnollisen GLP-1:n.
Kestää DPP-4:n hajoamista, puoliintumisaika 2,4 tuntia, pitkäkestoinen signalointireittien aktivointi.
Heikko positiivinen varaus, tunkeutuu helposti solukalvoon ja kerääntyy sytoplasmaan ja organelleihin.
Viitetietolähde:
- Mekanismi, jolla eksenatidi estää pyroptoosia ja parantaa maksan insuliiniresistenssiä PPAR δ:n eston avulla. Biotekniikka, 2026
- Eksenatidi parantaa maksan steatoosia ja heikentää rasvamassaa ja FTO-geenin ilmentymistä PI3K-signalointireitin kautta alkoholittomassa rasvamaksasairaudessa. PMC, 2024
- Eksenatidi vaimentaa alkoholitonta{0}}steatohepatiittia estämällä pyroptoosin signaalireittiä. Endokrinologian rajat, 2021
--solujen neogeneesin säätely: edistää esiastesolujen transdifferentiaatiota
Aikuisen haima sisältää multipotentteja esiastesoluja (tiehyepiteeli, acini, alfa-solut), joiden neogeneesi on alhainen fysiologisissa olosuhteissa; Diabeteksen neogeneesi estyy, eikä se voi kompensoida apoptoosin menetystä. Eksenatidi aktivoi tehokkaasti beetasolujen regeneraatiota ja on keskeinen mekanismi beetasolupopulaation täydentämisessä.

Eksenatidin molekyylimekanismi edistää --solujen neogeneesiä

Aktivoi haiman esiastesolujen kantasoluja
Polku: cAMP PKA CREB- ja PI3K Akt -reitit aktivoivat synergistisesti - soluspesifisiä transkriptiotekijöitä, kuten Ngn3, Pdx-1 ja Nkx6.1.
Vaikutus: Kanavan epiteelin kantasolut erilaistuvat kantasolujen saamiseksi, mikä käynnistää --solujen erilaistumisohjelman.
Edistää alfa-solujen erilaistumista beetasoluiksi
Mekanismi: PCSK1:n ja Pax4:n tehostaminen, alfasolumarkkerigeenien (Arx, Glucagon) esto ja alfasolun kohtalon siirtymisen edistäminen beetasoluiksi.
Todisteet: db/db-hiirillä Exenatide lisää alfa-solujen erilaistumisnopeutta 3-4 kertaa, ja vastasyntyneiden beetasolujen osuus saavuttaa 20-30%.
Säätelee haiman mikroympäristöä
Estävät haiman fibroosia ja tulehdusta, parantavat solunulkoista matriisia (ECM) ja tarjoavat sopivan mikroympäristön angiogeneesille.
SDF-1:n säätely tehostaa esiastesolujen kohdistamista ja erilaistumista.
Biologisen kellon yhteistoiminnallinen säätely
Eksenatidi synkronoi haiman vuorokausikellon, aktivoi CLOCK/BMAL1:n ja tehostaa rytmisesti neogeneesiin liittyvien geenien ilmentymistä.

--solujen neogeneesin patologiset vaikutukset

Eläinmalli: db/db ja runsaasti{0}}rasvaisia ruokittujen hiirten eksenatidihoito 8–12 viikon ajan johti 50–70 prosentin lisäykseen vastasyntyneiden beetasolujen määrässä ja lisäsi merkittävästi insuliinipositiivisia soluja haimassa.
Solumalli: Indusoimalla ihmisen haiman kanavasolujen ja iPS-solujen erilaistumisen beetasoluiksi, Exenatide lisää erilaistumistehokkuutta yli 60 %.
Viitetietolähde:
- Maksan vuorokausirytmiä säätelevän eksenatidin molekyylimekanismin tutkimus. Kiinan farmakologinen tiedote, 2024
- GLP-1-reseptorin agonisti, eksenatidi, antoaika vaikuttaa eri tavalla vuorokausirytmeihin diabeettisissa db/db-hiirissä. Kentuckyn yliopiston lääketieteellinen korkeakoulu, 2024
- Mekanismi, jolla eksenatidi estää pyroptoosia ja parantaa maksan insuliiniresistenssiä PPAR δ:n eston avulla. Biotekniikka, 2026
Usein kysytyt kysymykset
K: Miksieksenatidisuspensioaiheuttaako joskus ohimenevän verensokerin nousun heti injektion jälkeen?
+
-
V: Mikropalloformulaatio vapauttaa pienen ensimmäisen eksenatidipurskeen, joka voi tilapäisesti hidastaa mahalaukun tyhjenemistä voimakkaammin ja muuttaa varhaista insuliinin/glukagonin dynamiikkaa. Joillakin henkilöillä tämä nostaa väliaikaisesti verensokeria, ennen kuin vakaa terapeuttinen vaikutus valtaa.
K: Voiko injektiosuspensio vaikuttaa ihon kollageeniin tai elastiiniin paikallisesti pitkäaikaisessa toistuvassa{0}}käytössä?
+
-
V: Kyllä. Pitkäkestoisesti vapautuvat{1}}mikropallot tuottavat lievän kroonisen paikallisen tulehduksen. Kuukausien kuluessa tämä voi muuttaa ihon fibroblastien toimintaa hienovaraisesti, mikä johtaa lievään paikalliseen paksuuntumiseen tai ihon kimmoisuuden vähenemiseen toistuvissa injektiokohdissa, mitä ei havaita välittömästi vapautuvilla-formulaatioilla.
K: Miksi munuaisten vajaatoiminta vaikuttaa vähemmän eksenatidiin verrattuna välittömästi{0}}vapauttavaan eksenatidiin?
+
-
V: Sen jatkuva alhainen{0}}tasoinen vapautuminen välttää korkeat plasman huippupitoisuudet. Koska GLP-1-reseptoriagonistit poistuvat osittain munuaisten kautta, pienemmät piikit vähentävät munuaisten suodatuskuormitusta, mikä tekee siitä anteeksiantavamman lievän tai kohtalaisen munuaisten vajaatoiminnan yhteydessä.
K: Häiritseekö suspensiopohja yleisiä hormoni- tai vasta-aineimmunomäärityksiä?
+
-
V: Polymeerimikropallot ja suspendoiva vehikkeli voivat sitoutua heikosti määritysvasta-aineisiin tai aiheuttaa epäspesifisen taustasignaalin. Tämä voi johtaa lievään aliarviointiin tai matriisivaikutuksiin joissakin immuunimäärityksissä, jos sitä ei huomioida kunnolla.
K: Miksi eksenatidilla on pienempi takyfylaksia (pienempi vaste ajan myötä) riski?
+
-
V: Vakaa, jatkuva reseptoristimulaatio välttää suuret pitoisuusvaihtelut, jotka havaitaan kahdesti kerran annettaessa. Tämä vähentää GLP-1-reseptorin sisäistämisen ja herkistymisen esiintymistiheyttä, mikä auttaa säilyttämään glykeemisen tehon pidempään joillakin potilailla.
Suositut Tagit: eksenatidisuspensio, toimittajat, valmistajat, tehdas, tukkumyynti, osta, hinta, irtotavarana, myytävänä









